ALCANOS
Son hidrocarburos saturados estan formados exclusivamente por carbono e hidrógeno y únicamente hay enlaces sencillos en su estructura.
PERO ¿QUE SON LOS HIDROCARBUROS SATURADOS?
- Su formula general es CnH2n+2 ( donde ¨n¨ es el numero de carbonos que nos indican y esta formula ayuda a indicar cuantos hidrógenos hay en ese compuesto.) Por ejemplo: C4 entonces cuantos hidrógenos
- tiene? H2*n+2 = H2*4 + 2 = 10 hidrógenos. C4H10
- TIENEN ENLACES COVALENTES SENCILLOS.
- QUE SIGNIFICA ¨SATURADOS¨? significa que tienen todos los hidrógenos por carbono.
- OBTENCIÓN: petroleo y gas natural.
- USOS: combustibles y sustrato para síntesis químicas.
- SU HIBRIDACIÓN ES Sp3.
PROPIEDADES DE LOS ALCANOS:
- el estado físico de los 4 primeros alcanos: METANO, ETANO, PROPANO Y BUTANO es GASEOSO.
- Del pentano al hexadecano son Liquidos y a partir del heptadecano son sólidos.
- el punto de fusión, de ebullicion y la densidad aumentan conforme aumenta el número de átomos de carbono.
- Insolubles en agua.
- Pueden emplearse como disolverse para sustancias poco polares como grasas, aceites y ceras.
- El principal uso de los alcanos es como combustibles debido a la gran cantidad de calor que se libera en esta reacción.
CICLOALCANOS
Los cicloalcanos son alcanos que tienen los extremos de la cadena unidos, formando un ciclo. Tienen dos hidrógenos menos que el alcano del que derivan, por ello su fórmula molecular es CnH2n (donde en cambio de la formula anterior aqui solo se multiplica el numero de átomos de carbonos * 2). Se nombran utilizando el prefijo ciclo seguido del nombre del alcano.

ISOMERÍA: son compuestos distintos con la misma fórmula molecular.
- ISOMERIA DE FUNCIÓN: cuando las dos moléculas presentan diferentes grupos funcionales.
- ISOMERIA DE CADENA: si varias sustancias isómeras tienen la misma función pero diferente cadena o esqueleto carbonado.
- ISOMERIA DE POSICIÓN: cuando tienen la misma funcion e identica cadena carbonada, se van a diferenciar en la posición del grupo funcional.
- METAMERAS: tienen el mismo grupo funcional sustituido de formas distintas.
- ISOMERIA CIS-TRANS: distinta formula desarrollada.

- ISOMERIA ÓPTICA: solo se observa distinta distribucion espacial (en 3 dimensiones) de los grupos unidos a un átomo de carbono, para que haya isomeros ópticos es necesario que os 4 sustituyentes unidos a un átomo de carbono sean distintas. ¨carbono asimetrico¨
- Se asigna un orden de prioridad a los grupos por # ÁTOMICA. si 2 de ellos fueron el mismo átomo el orden se determina por la prioridad de sus sustituyentes.
- Se sitúa el sustituyente 4 hacia atrás y se observa el triangulo que forman los otros 3. Si el orden 1-2-3 sigue las agujas del reloj el isomero se determina R y si sigue al contrario se determina S.
HIDROCARBUROS: NOMENCLATURA
- HIDROCARBUROS ALIFATICOS ACÍCLICOS: ALCANOS
ALCANOS NO RAMIFICADOS O LINEALES
Para su nombre el prefijo que indica el # de carbonos + -ano. por ejemplo: hex + ano = hexano.

NOMBRES DE RADICALES SENCILLOS
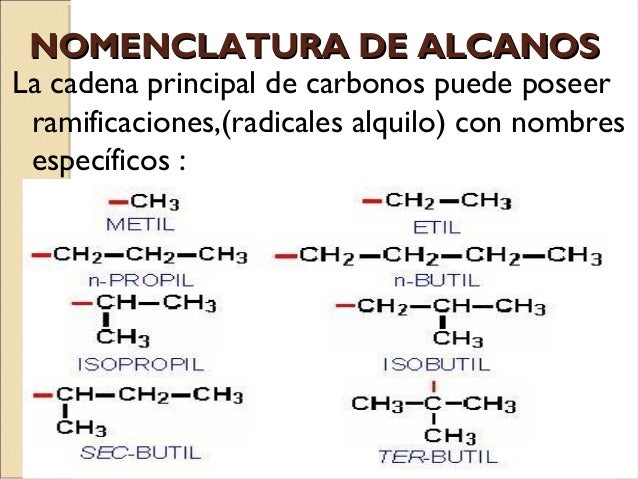
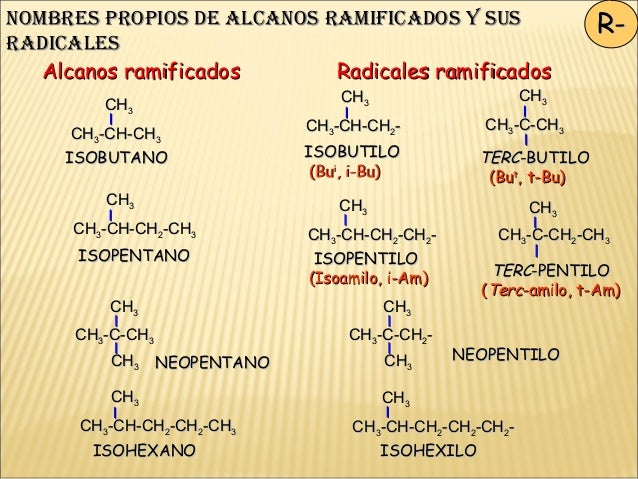
ELECCION DE LA CADENA PRINCIPAL
1. la de mayor longitud ( mayor # de atomos de carbono)
2. en caso de varias opciones: mayor # de cadenas laterales o radicales.
radicales con posiciones mas bajas.
mayor # de carbonos en cadenas laterales mas cortas.
cadenas laterales menos ramificadas.
NOMENCLATURA
1. elegir la cadena principal mas larga.
1.1 se elige la cadena de mayor numero de atomos de carbono.
1.2 aquella de mayor numero de cadenas laterales.
1.3 aquella de cadenas laterales con localizadores o posiciones mas bajas.
1.4 aquella de mas carbonos en la cadena lateral mas pequeña.
NUMERACIÓN
2.1 numeros mas bajos a los sustituyentes.
2.2 numeros mas bajos a los sustituyenes por orden alfabetico.
NOMBRE
localizadores - sustituyentes + nombre alcano
(cadenas laterales) (cadena principal)
3.1 se antepone los nombres de los sustituyentes por orden alfabetico acompañados de su localizador o posicion.
3.2 sustituyentes repetidos en el mismo y/o otro carbono repiten y utilizan prefijos multiplicativos (di-, tri-, tetra-, etc)
3.3 los prefijos multiplicativos no se alfabetizan.
3.4 los prefijos n-, sec-, terc- no se alfabetizan.
3.5 los prefijos iso, neo y ciclo si se alfabetizan y se escriben sin guion.
3.6 para nombrar a los radicales ramificados se aplican as mismas reglas:
- El C1 es el unido a la cadena principal.
- los localizadores se escriben com primas o junto con el nombre del sustituyente entre parentesis.
- se alfabetiza el prefijo multiplicador del radical sencillo.
- cuando hay varios radicales complejos se utiliza: bis, tris, tetrakis, etc, sin alfabetizar.

HIDROCARBUROS ALIFATICOS CICLICOS
1. se antepone el prefijo ciclo- al nombre del alacano de igual numero de carbonos.
1.2 los radicales se nombran cambiendo -ano por -ilo.
1.3 cicloalcanos sustituidos: se utilizan las mismas reglas que para alcanos, cuando solo hay un sustituyente, no se precisa localizador.
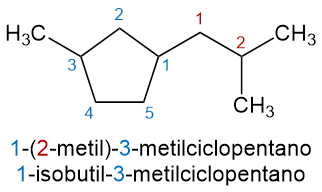
1.4 algunos ejemplos de cicloalcanos por enlaces C-C
con ciclos iguales:
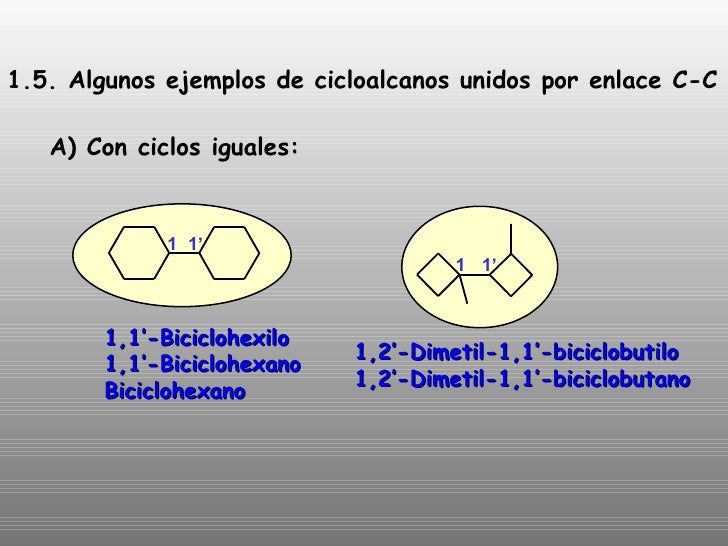
ciclos diferentes:

PROPIEDADES FISICAS
- Presentan serie homologa.
- los puntos de ebullicion aumentan la cadena.
- son menos densos de todos los grupos de moleculas organicas.
- insolubles en agua.
PROPIEDADES QUIMICAS
- falta de reactividad.
- son atacados por el oxigeno a elevadas temperaturas.
- se descomponen por temperaturas altas en ausencia de oxigeno.
- PIROLISIS: se efectua la escision de alcanos de peso molecular grande en moléculas de menor tamaño.
ESTEREOQUÍMICA DE LOS ALCANOS
ANÁLISIS CONFORMACIONAL Y PROYECCIONES DE NEWMAN
EQUILIBRIO CONFORMACIONAL
se puede transformar un confórmero en otro mediante la rotación en torno a enlaces simples, lo que no es posible en los esteroisómeros donde es necesario romper enlaces para transformar un en otro. 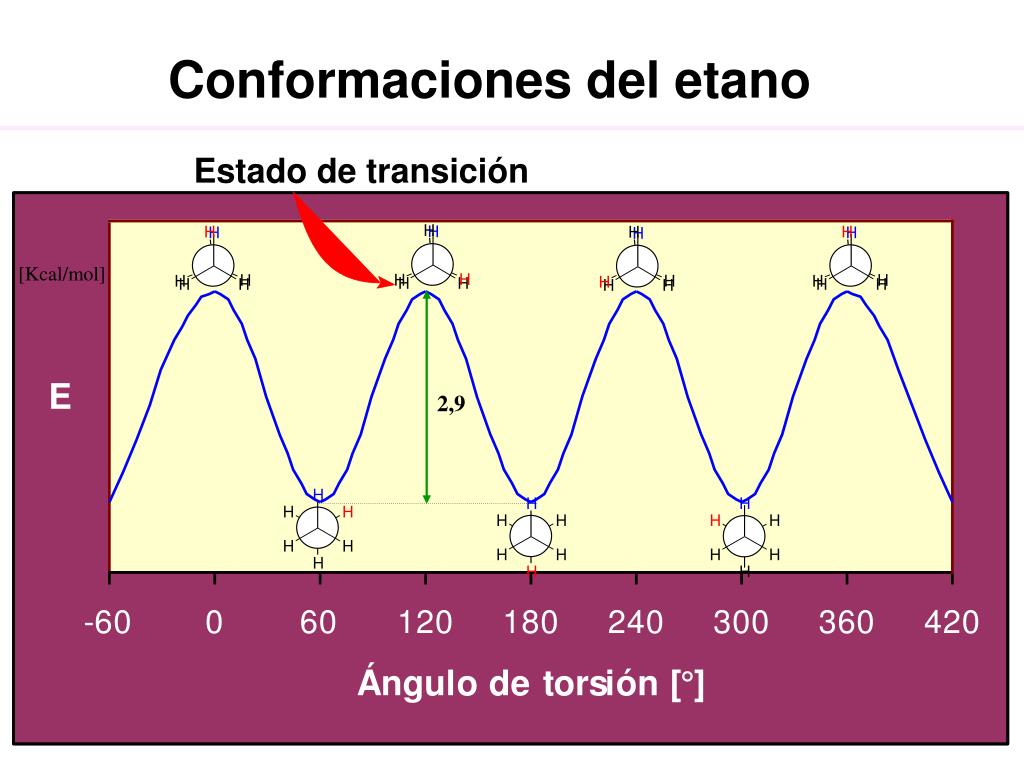 los diversos rotámeros del etano no poseen la misma energía potencial.
los diversos rotámeros del etano no poseen la misma energía potencial.
 los diversos rotámeros del etano no poseen la misma energía potencial.
los diversos rotámeros del etano no poseen la misma energía potencial. - al girar un grupo metilo alrededor del eje C-C, empezando a partir de la conformacin alternada, la distancia entre los hidrogenos disminuye, dando lugar a un aumento en la repulsion entre los pares enlazantes de los enlaces C-H.
- en el punto de eclipse, la molécula tiene su contenido maximo de energia.
- el cambio de energia asociado a la rotacion alrededor de un enlace se llama energia rotacional o torsional.
- en este caso la superficie de energia potencial (SEP) es una funcion sinusoidal de periodo 120´ y una amplitud 2.9 kcal/mol.
todo esto son las proyecciones de Newman
aqui se explica mejor la conformacion del etano
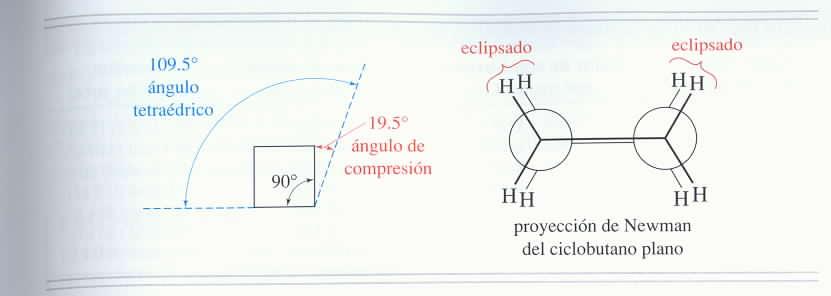
TENSION DE ANILLO DE UN CICLOBUTANO
La tension de anillo de un ciclobutano plano se debe a dos factores: la tension angular debida a la comprension de los angulos de enlaces desde el angulo tetraedrico de 109.5 grados hasta 90 grados y la tension torsional debida al eclipsamiento de los enlaces C-H.
La comprension para el butano es 19.5 grados. la tension angular t la tension torsional explican la alta reactividad de los anillos de cuatro átomos de carbono.
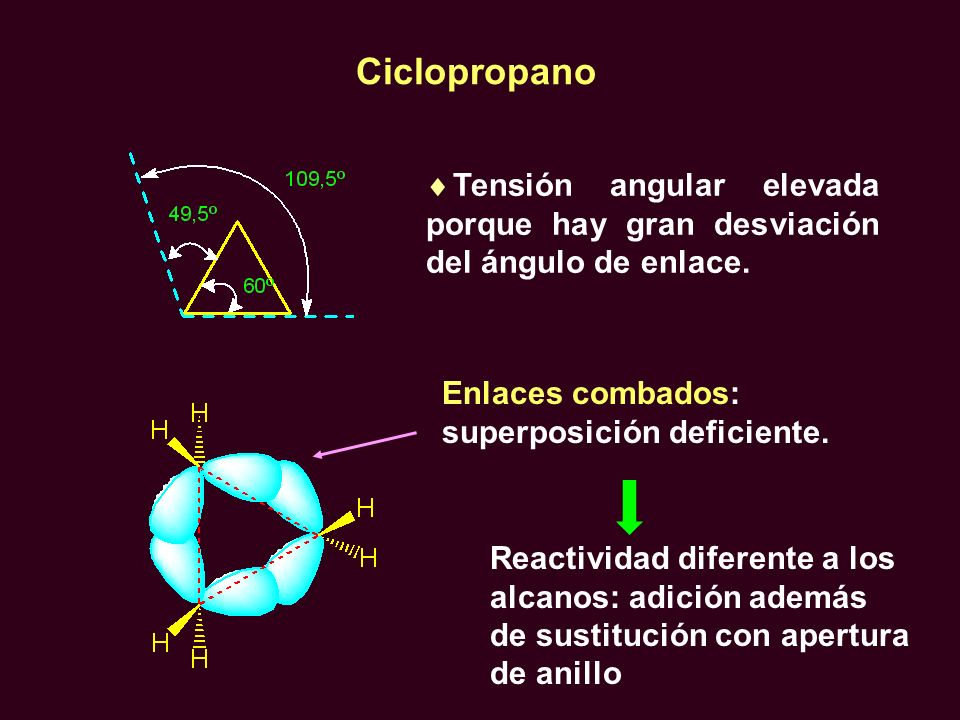
CONFORMACIONES DEL CICLOPROPANO
Todos los enlaces C-C estan eclipsados, generando una tensin torsional que contribuye a la tension total de anillo. la tension angular y la tension torsional en el ciclopropano hacen que el tamaño de este anillo sea extremadamente reactivo.
CONFORMACIONES DEL CICLOPENTANO
la conformacion del ciclopentano esta ligeramente doblada, como la forma de un sobre. esta conformacion plegada reduce el eclipsamiento de los grupos CH2 adyacentes.

CONFORMACIONES DEL CICLOHEXANO
CONFORMACION DE BOTE DE CICLOHEXANO
la conformacion de barca simetrica del ciclohexano, el eclpisamiento de los enlaces da lugar a tension torsional. en la molecula representada, la barca se retuerce y se forma la barca torcida, una conformacion con los enlaces menos eclipsados y con menor interaccin entre los dos hidrogenos mástil.
- el análisis conformacional del ciclohexano indica que las barreras del potencial son mayores y por lo tanto les podemos medir facilmente en comparacion con las otras familias.
- el conformero silla es el mas estable.
- las otras conformaciones bote y twist (bote retorcido) son menos estables.
ejercicios
en este video se les dara 10 ejercicios y se resolverán, trate de hacerlo antes de que le proporcionen la respuesta.

Seria importante colocar algunos ejercicios de nomenclatura
ResponderBorrar